|
Аптечный контроль. Что затронет в ближайшие годы фармацевтический рынок России и каждого из нас?
Главная /
Архив номеров / 2016 / Выпуск №06 (59) / Аптечный контроль. Что затронет в ближайшие годы фармацевтический рынок России и каждого из нас?
Рубрика:
БИТ.Медицина
Facebook
Мой мир
Вконтакте
Одноклассники
Google+
Аптечный контроль
Что затронет в ближайшие годы фармацевтический рынок России и каждого из нас?
Только-только прошел бум на рынке ретейла, связанный с внедрением системы ЕГАИС, суть которой заключается в сквозном контроле оборота алкогольной продукции от производителя до кассы магазина, как пришла пора серьезных изменений для производителей и продавцов лекарственных препаратов
 30 ноября 2015 года Минздрав России утвердил концепцию создания государственной информационной системы мониторинга движения лекарственных препаратов (приказ №866 «Об утверждении концепции создания федеральной государственной информационной системы мониторинга движения лекарственных препаратов от производителя до конечного потребителя с использованием маркировки»). 30 ноября 2015 года Минздрав России утвердил концепцию создания государственной информационной системы мониторинга движения лекарственных препаратов (приказ №866 «Об утверждении концепции создания федеральной государственной информационной системы мониторинга движения лекарственных препаратов от производителя до конечного потребителя с использованием маркировки»).
Федеральная государственная информационная система мониторинга движения лекарственных препаратов (ФГИС МДЛП) будет отслеживать их перемещение от производителя до конечного потребителя с использованием индивидуальной и групповой кодированной маркировки и идентификации упаковок. Глобальная цель – контроль качества лекарств, находящихся в обращении, и борьба с их фальсификацией.
Надо сказать, что сама тема мониторинга не нова. С 1 июля 2014 года производители и импортеры лекарственных средств обязаны предоставлять в Росздравнадзор сведения о сериях и партиях лекарственных средств, поступающих в страну. Однако до сих пор это был выборочный контроль (так называемая АИС Росздравнадзора, введенная в конце 2011 года).
Разработать необходимый функционал системы и внедрить ее в качестве пилотного проекта Минздрав планирует до 31 октября 2016 года, а уже с 1 января 2019-го предполагается приступить к полнофункциональной эксплуатации ФГИС МДЛП, предусматривающей поэтапное внедрение.
| Трудно представить, но сейчас более 20% лекарственных средств в системе ОМС поставляется не централизованно, а «самозакупом» из‑за сложностей в принятом регламенте |
В этом пилотном проекте участвует сейчас целый регион – Белгородская область, а из участников со стороны производителей – один из крупнейших фармдистрибуторов России – компания «Катрен», чей годовой оборот составляет 203 млрд рублей.
На протяжении двух последних лет некоммерческое партнерство «Регистр лекарственных средств» совместно с компанией «СофТраст» выступало инициатором и разработчиком системы регионального мониторинга в рамках построения локального фрагмента пилотного проекта.
Если говорить о текущей ситуации, то узких мест, требующих структурного единого подхода к их устранению, довольно много.
Это и ситуация, когда единый классификатор лекарственных средств существует только в системе ДЛО, и то, что стационары ведут персонифицированный учет медикаментов, но источником номенклатуры является накладная поставки, которая сопоставляется по торговым наименованиям.
Трудно представить, но сейчас более 20% лекарственных средств в системе ОМС поставляется не централизованно, а «самозакупом» из-за сложностей в принятом регламенте, когда от процедуры оформления заявки до поставки нужного препарата могут пройти месяцы, тогда как «лекарства нужны сегодня».
При этом невозможно получить автоматически ни перераспределения медикаментов между ЛПУ, ни сводного анализа с данными по потребностям в разрезе препарата, региона, врача и пациента. И финансисты постоянно выказывают недовольство на претензии медиков о недостаточности финансирования лекарственного обеспечения и требуют расшифровки потребности «до упаковки и пациента».
Что получит государство
Перспективы, открывающиеся перед регулятором фармрынка (Минздрав), поистине впечатляют.
Автоматизированная система позволит проследить истории движения препарата от момента выпуска в обращение до конечного потребителя; контролировать отпуск и адресность движения, а также использование отдельных групп препаратов; проверять сроки годности лекарств, находящихся в обращении.
Также ФГИС МДЛП должна обеспечить мониторинг изъятия из обращения недоброкачественных, фальсифицированных и незарегистрированных лекарств, мониторинг процесса уничтожения лекарств в целях предотвращения их поступления в обращение и предоставить возможность участникам системы получать различные отчеты и аналитику в рамках своих полномочий.
| Залог работающей системы – это выстраивание иерархии, где будут федеральный, региональный и локальный уровни |
Все это поможет сделать более эффективной задачу лекарственного и медицинского обслуживания населения. Одновременно это усилит контроль над расходованием бюджетных средств, повысит точность планирования потребностей в дорогостоящих и скоропортящихся лекарственных средствах.
В качестве одного из эффектов, который ожидает получить государство при внедрении ФГИС МДЛП, эксперты называют также снижение затрат на лекарственное обеспечение, сокращение количества ошибок распределения персоналом медпрепаратов на сестринском посту и увеличение степени достоверности данных отчетов и скорости их построения.
Для всех и каждого
Надо сказать, что сейчас предполагается, что доступ к системе с использованием веб-интерфейса или мобильного приложения получат все россияне. Информацией можно будет воспользоваться при покупке препаратов, чтобы проверить их подлинность, данные о производителе, а также срок годности.
| Кстати
Сегодня, по данным Росздравнадзора, российский фармацевтический рынок состоит из следующих сегментов:
- 1985 организаций-дистрибуторов (2159 объектов);
- 25 631 организация розничного сегмента (74 057 объектов, в том числе 25 043 аптеки, 26 895 аптечных пунктов, 260 аптечных киосков, 1870 индивидуальных предпринимателей, 19 989 ФАПов, амбулаторий и кабинетов общей практики, осуществляющих розничную торговлю лекарственными препаратами).
|
По аналогии со все той же системой ЕГАИС достаточно будет сканировать QR-код, чтобы получить всю информацию о лекарственном средстве (кем и когда оно было произведено, куда поставлялось и каков срок годности).
На конференции, прошедшей в рамках недели здравоохранения осенью 2015 года, руководитель НП РЛС Геннадий Вышковский назвал основные сложности, которые необходимо решить для успешного внедрения информационной системы. Он видит их прежде всего в отсутствии документов для нормализации информации (консолидация, синхронизация, гармонизация).
А где GTIN?
Если говорить о первых шагах, которые необходимо будет сделать производителям (и поставщикам) лекарственных средств, то это внедрение маркировки продукции. Сегодня международный идентификатор GTIN может принадлежать различным упаковкам1.
Мировой опыт внедрения мониторинга отсылает нас к 2006 году, когда на конгрессе под эгидой ВОЗ было принято решение о старте построения системы. Документ, на который сейчас опираются международные производители (среди них Pfizer, Sanofi и др.), внедрившие уже необходимую систему многоуровневой маркировки, – «Глобальный стандарт отслеживаемости».
Залог работающей системы – это выстраивание иерархии, где будут федеральный, региональный и локальный уровни.
Если же вернуться к вопросу идентификации, то есть потребность в требованиях по идентификации продукта (Идентификационный номер, Атрибуты продукта, Штриховой код, Маркировка единичной дозы) и отслеживаемости (Сериализация, Система проверки подлинности/происхождения).
В сфере здравоохранения существуют определенные требования/особенности к данным и их носителям. Так, для маркировки медицинского инструмента необходимо применение метода DPM (прямой маркировки на металле/пластике).
Другой особенностью является малая площадь, которую можно отвести для штрих-кода. Для этого рекомендуется использовать несколько видов штрих-кодов:
- линейный GS1-128 и GS1 DataBar, если позволяет упаковка;
- 2D GS1 DataMatrix, который является предпочтительным вариантом, если необходимо передать с помощью кода большой объем данных на маленьком пространстве.
Так выглядит система идентификации медицинских препаратов (см. рис. 1).
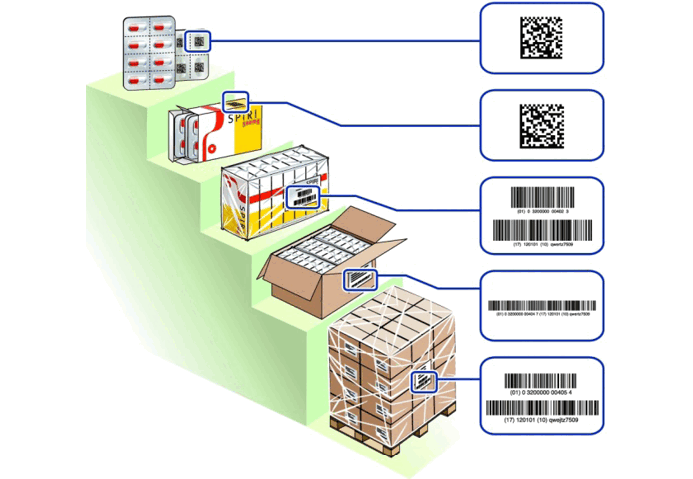
Рисунок 1. Система идентификации медицинских препаратов
С точки зрения повышения безопасности система предлагает следующие взаимодополняющие элементы (см. рис. 2).
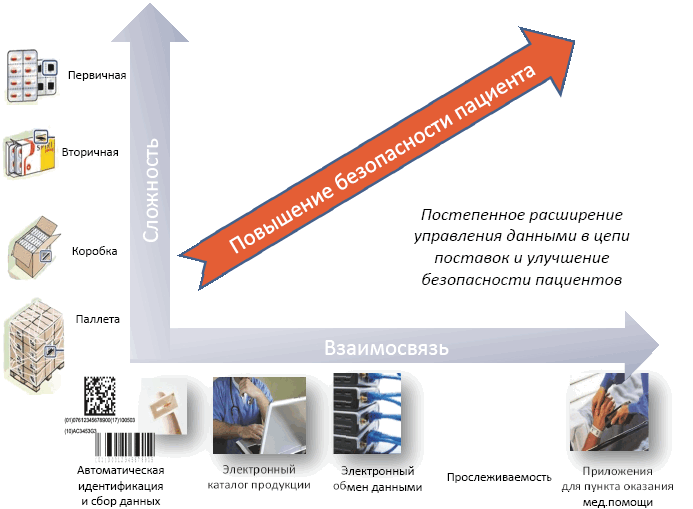
Рисунок 2. С точки зрения повышения безопасности система предлагает следующие взаимодополняющие элементы
Единые стандарты на протяжении всей цепочки от производителя до палаты/аптеки в конечном счете служат улучшению безопасности пациентов и эффективности цепи поставок.
В одном из ближайших номеров журнала мы планируем познакомить вас с ходом проведения российского пилотного проекта, рассказав подробнее о том, что затронет в ближайшие годы не только весь фармацевтический рынок России, но практически каждого.
Елена Алексеева
1 Хайлефлокс – таблетки, покрытые пленочной оболочкой 500 мг, 5 шт. – блистеры из ПВХ/алюминия (1) – пачка картонная (GTIN – 8904102200080).
Хайлефлокс – таблетки, покрытые пленочной оболочкой 500 мг, 10 шт. – блистеры из ПВХ/алюминия (1) – пачка картонная (GTIN тот же – 8904102200080). В начало⇑
Facebook
Мой мир
Вконтакте
Одноклассники
Google+
Комментарии отсутствуют
Комментарии могут отставлять только зарегистрированные пользователи
|